Читать книгу - "Абсолютный минимум. Как квантовая теория объясняет наш мир - Майкл Файер"
Следующим идёт углерод (C, 6) с шестью электронами. Теперь в игру вступает правило Хунда, и мы помещаем шестой электрон на 2py-орбиталь, следуя схеме, представленной на рис. 11.3. Следующий элемент — азот (N, 7). Согласно правилу Хунда, седьмой электрон N заселяется на 2pz-орбиталь, чтобы ни один из электронов на p-орбиталях не был спаренным. Кислород (O, 8) имеет восемь электронов. Восьмой электрон должен быть спаренным, поскольку из первых семи электронов два занимают 1s-орбиталь, ещё два — 2s и по одному электрону находится на каждой из 2p-орбиталей. Чтобы избежать спаривания спинов, надо поместить восьмой электрон на 3s-орбиталь, которая требует значительно более высокой энергии. Поэтому, как и на рис. 11.3, восьмой электрон заселяется на 2px-орбиталь. Фтор (F, 9) обладает девятым электроном, который располагается на 2py-орбитали. Наконец, неон (Ne, 10) завершает период n=2 с оболочкой из 10 электронов. Десятый электрон заселяется на 2pz-орбиталь.
Электронная конфигурация неона изображена на рис. 11.5. Ни один дополнительный электрон не может заселиться на вторую оболочку (орбитали с n=2) без нарушения принципа Паули. Как будет объяснено далее, элементы He, Ne, Ar, Kr и т. п., занимающие последнюю колонку в правой части Периодической таблицы, — особые. Эти элементы называются благородными газами. Все они обладают замкнутыми (заполненными) оболочками, то есть со следующего элемента, имеющего на один электрон больше, начинают заполняться орбитали с квантовым числом n на единицу больше, а значит, обладающие значительно более высокой энергией.
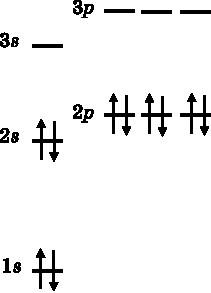
Рис. 11.5. Электронная конфигурация атома неона (Ne, 10). Вторая оболочка заполнена
Теперь мы готовы использовать диаграмму энергетических уровней (см. рис. 11.1) и наши три правила расселения электронов по энергетическим уровням для объяснения строения Периодической таблицы и свойств элементов. В следующих главах будет подробно разбираться вопрос о том, что удерживает атомы вместе в составе молекул, однако очень многое можно понять на основе поразительно простого правила: атомы будут захватывать или отдавать электроны, стремясь к ближайшей конфигурации с заполненной оболочкой. Замкнутые электронные оболочки — это электронные конфигурации благородных газов, которые располагаются в правой колонке Периодической таблицы. Конфигурации с замкнутыми оболочками исключительно стабильны. Благородные газы, также называемые инертными, обладают заполненными оболочками и в основном химически инертны. Благородные газы с малыми атомными номерами — гелий, неон и аргон — вообще не образуют химических соединений. Благородные газы с более высокими атомными номерами в особых условиях можно заставить образовать небольшое число соединений. Атомы, отличные от благородных газов, меняются в направлении, приближающем их к образованию устойчивой замкнутой электронной оболочки.
Есть два способа, которыми атом может изменить число своих электронов, чтобы достичь замкнутости электронной оболочки. Первый способ — стать положительным ионом (катионом) или отрицательным ионом (анионом). Атом отдаёт один или больше своих электронов и становится положительно заряженным (катионом) или захватывает дополнительные электроны и становится отрицательно заряженным (анионом). Альтернативный путь для атома состоит в том, чтобы совместно использовать электроны с одним или несколькими другими атомами. Когда два или более атома объединяют электроны, это действует так, как если бы каждый атом обладал необходимыми ему электронами. Тем самым атом с меньшим числом электронов, чем требуется для образования следующий замкнутой электронной оболочки, получает нужное их число, но то же самое происходит и с другими атомами, задействованными в совместном использовании.
Когда атомы совместно используют электроны, чтобы получить такое их число, которое требуется для образования следующей замкнутой оболочки, это совместное использование удерживает атомы вместе. Совместное использование электронов приводит к тому, что энергия соединённых атомов становится ниже энергии отдельных недозаполненных оболочек. Это уменьшение энергии связывает атомы друг с другом. Такой тип химической связи называется ковалентной связью. Ковалентные связи представляют собой основной тип связи в химии. Природа ковалентной связи подробно разбирается в главе 12 на примере простейшей молекулы — водорода, а более сложные молекулы обсуждаются в последующих главах.
Переходя к обсуждению свойств атомов, основанному на Периодической таблице, начнём с водорода. Водород — это особый атом, поскольку у него лишь один электрон, и это первый элемент в Периодической таблице. В первой строке Периодической таблицы гелий имеет заполненную оболочку с двумя электронами на 1s-орбитали. Водород может обзавестись замкнутой конфигурацией оболочки, как у гелия, позаимствовав электрон у другого атома в порядке совместного использования. Например, один атом водорода может совместно использовать электрон с другим атомом водорода, образовав молекулу водорода. Обозначение молекулы водорода H2. Индекс указывает, сколько атомов данного типа содержится в молекуле. Благодаря совместному использованию электронов каждый из атомов водорода ощущает себя так, как если бы у него было два электрона, то есть замкнутая электронная оболочка, подобная той, что имеется у гелия.
Как мы увидим далее, водород может образовывать другие молекулы, но поскольку ему требуется лишь один электрон, чтобы получить заполненную электронную оболочку, как у гелия, он может образовывать одну химическую связь. Гелий имеет замкнутую оболочку. Он не способен образовывать какие-либо химические связи. Не существует молекул, в которые входил бы атом гелия. Почему именно так происходит, описывается в главе 12. Гелий замыкает первый период.
Следующий элемент — это литий (Li), который располагается в Периодической таблице непосредственно под H. Li может получить заполненную конфигурацию оболочки, как у гелия, отдав электрон. Поэтому Li образует положительные ионы Li1+. В твёрдом виде Li является металлом. Металлы способны проводить электричество, а значит, электроны могут свободно перемещаться от одного атома к другому. Природа металлов и электропроводности будет обсуждаться в главе 19. Металлы отличаются тем свойством, что, будучи одиночными атомами, они легко могут отдать один или несколько электронов. Электрон, отданный литием, должен куда-то деться. Он перейдёт к другому атому, которому нужно получить электрон, чтобы образовать отрицательный ион. Таким образом, для образования иона Li1+ литию нужен партнёр (см. обсуждение ниже, где мы добираемся до другой стороны Периодической таблицы).
Прочитали книгу? Предлагаем вам поделится своим впечатлением! Ваш отзыв будет полезен читателям, которые еще только собираются познакомиться с произведением.
Оставить комментарий
- Яна29 май 16:31Двойное отцовство - Таня ВолодинаКлассная история! Не похожа ни на одну про отношения МЖМ, которые я читала до этого. Очень приятные харизматичные герои, мастерски написанные характеры главных
- Аида06 май 10:49Дикарь королевских кровей. Книга 2. Леди-фаворитка - Анна Сергеевна ГавриловаЧитала легко, местами хоть занудно. Но, это лучше, чем 70% подобной тематики произведений.
- вера02 май 00:32Сокровище в пелёнках - Ирина Агуловатекст не четкий трудно читать наверное надоест сброшу книгу может посоветуете как улучшить
- Калинин максим30 апрель 10:11Время Темных охотников - Евгений ГаглоевНедавно прочитал книгу «Время тёмных охотников» и хочу поделиться своими впечатлениями. Автор создал увлекательный мир, полный тайн и загадок. Сюжет затягивает с первых







